Caratterizzazione di nanomateriali in matrici alimentari
Caratterizzazione di nanomateriali in matrici alimentari
Identificazione e verifica della loro presenza
Marco Roman, Federico Benetti
Le nanotecnologie offrono grandi prospettive di innovazione per l’industria del settore agroalimentare. La nanoscala, infatti, conferisce ai materiali proprietà chimico-fisiche peculiari da cui possono derivare vantaggi, quali una maggiore reattività chimico/biologica che ne consente l’impiego nella produzione, nel processamento e nella conservazione degli alimenti, nella realizzazione di additivi ed ingredienti, e nello sviluppo di materiali innovativi a contatto con il cibo.
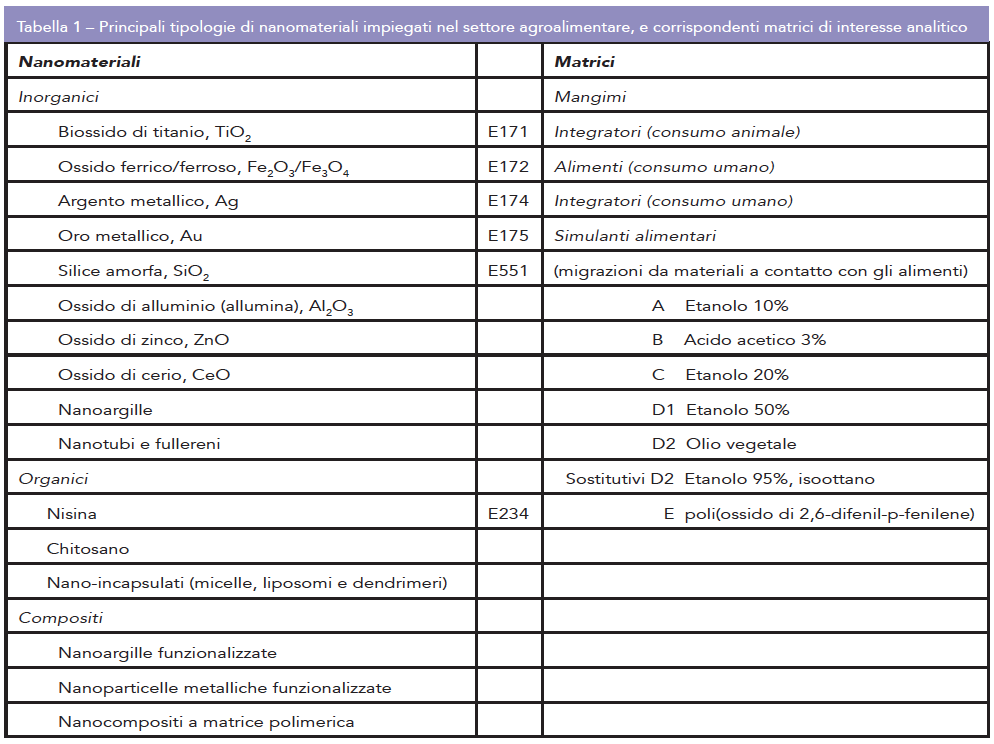
La maggior parte dei nanomateriali utilizzati nel settore agroalimentare sono inorganici (Tab.1), con metalli e ossidi metallici presenti nel 55% delle applicazioni, e nanotubi, fullereni ed argille impiegati nel 12% dei casi (1). I nanomateriali a base organica, come ad esempio micelle, liposomi o dendrimeri, vengono per lo più utilizzati per incapsulare e veicolare additivi, nutrienti o farmaci e rappresentano il 26% delle applicazioni. Vi sono infine i materiali nanocompositi, costituiti da strutture inorganiche come le argille, la cui superficie viene modificata o funzionalizzata con componenti organiche o polimeriche modificate o funzionalizzate con componenti nanometriche per ottimizzarne le proprietà barriera o conferirvi attività antimicrobiche, e che costituiscono circa il 7% delle applicazioni.
A ciascuna tipologia di nanomateriale e modalità di utilizzo corrisponde uno scenario di esposizione per il consumatore, che può essere diretto nel caso di ingredienti e/o additivi costituiti da nanomateriali, o indiretto nel caso di nanoparticelle rilasciate negli alimenti dal materiale di confezionamento (2). Per entrambe le tipologie di esposizione, diretta e indiretta, è importante valutare la natura chimica, la quantità (esposizione) ed il comportamento del nanomateriale nell’alimento o nei simulanti alimentari. Come sottolinea la European Food Safety Authority (EFSA) nelle sue linee guida per la valutazione dell’esposizione ai nanomateriali (3), non è sufficiente caratterizzarli nella loro forma di materia prima in quanto a contatto con matrici biologiche potrebbero subire sostanziali trasformazioni chimico-fisiche che ne alterano l’impatto biologico. La capacità di identificare, quantificare e caratterizzare i nanomateriali negli alimenti e nei simulanti alimentari diventa quindi un requisito fondamentale per ottimizzarne l’efficacia, riducendo i rischi connessi al loro utilizzo in accordo con Raccomandazioni e Normative, come i Regolamenti (EU) n.1169/2011 e n.2283/2015 (4,5).
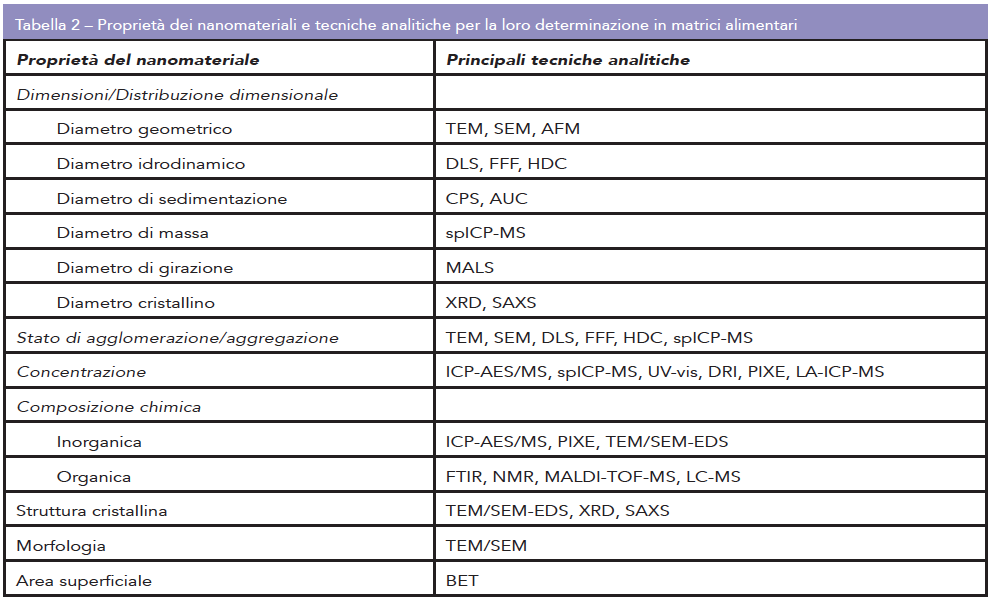
Essendo i nanomateriali definiti sulla base di un criterio dimensionale (2), determinarne le dimensioni è un requisito imprescindibile per la loro identificazione. Come riportato in Tabella 2, il concetto di “dimensioni” di un nanomateriale o nanoparticella ha diverse accezioni, tutte ugualmente adottabili, a cui corrispondono tecniche analitiche specifiche (6). In un contesto normativo dove un nanomateriale viene definito come …un materiale naturale, accidentale o prodotto intenzionalmente, contenente particelle libere o strutturate in aggregati/agglomerati con il 50% o più delle particelle aventi una distribuzione dimensionale compresa tra 1 nm e 100 nm. In alcuni casi e per ragioni di sicurezza la soglia del 50% può essere abbassata ad un valore compreso tra 1 e 50%, le tecniche di riferimento per la determinazione della distribuzione dimensionale di una popolazione di oggetti nanometrici sono la microscopia elettronica a trasmissione (TEM) e a scansione (SEM), che consentono di valutarne la morfologia, il diametro geometrico e la frequenza relativa di particelle che ricade nella definizione.
Il comportamento di un nanomateriale in matrici complesse come quelle alimentari è determinato da una grande varietà di caratteristiche chimico-fisiche che si influenzano reciprocamente, tra cui dimensioni e distribuzione dimensionale, morfologia, stato di aggregazione/agglomerazione, struttura cristallina, concentrazione e quantità totali, composizione chimica interna e superficiale, carica ed area superficiali (7). Se da un lato la scelta della proprietà di interesse condiziona la scelta della tecnica analitica per la sua determinazione (Tab.2), dall’altro il numero e l’interdipendenza delle proprietà impone l’integrazione di più approcci per ottenere informazioni adeguatamente complete. È altrettanto importante sottolineare che ciascuna tecnica per la caratterizzazione dei nanomateriali presenta limitazioni specifiche, spesso determinate dal modo in cui le componenti della matrice interferiscono con la proprietà misurata. Per questo motivo è a maggior ragione utile, quando possibile, utilizzare due o più tecniche per determinare una singola proprietà, in modo da consolidarne reciprocamente il risultato.
Queste considerazioni contribuiscono a rendere la caratterizzazione dei nanomateriali in matrici di interesse agroalimentare una frontiera anche per la ricerca, oltre che operativamente complessa e dispendiosa. L’adozione di approcci sperimentali standardizzati e strutturati, ad esempio organizzando le prove su basi gerarchiche e sequenziali, può aiutare sensibilmente ad ottimizzare il processo analitico, e a renderlo più accessibile ad un ambito rutinario.
Molti approcci analitici per la determinazione di nanomateriali in matrici e simulanti alimentari richiedono campioni liquidi, e pertanto un’estrazione preliminare dei nanomateriali dalle matrici solide o semi-solide. Tra queste tecniche, il dynamic light scattering (DLS) fornisce una misura del diametro idrodinamico di una popolazione di nanoparticelle, garantendo una buona precisione in un ampio intervallo dimensionale. Rapido ed economico, ma poco sensibile e inadatto a materiali polidispersi, il DLS è generalmente utilizzato per effettuare screening preliminari. Sulla stessa definizione di dimensione idrodinamica si basano le tecniche per la separazione su base dimensionale di nanoparticelle in sospensione, quali la field flow fractionation (FFF) e la cromatografia
idrodinamica (HDC). Rispetto al DLS, queste tecniche sono potenzialmente più sensibili per le basse concentrazioni e più affidabili per nanomateriali eterogenei e polidispersi, ma richiedono accoppiamento con opportuni rivelatori quali multiangle light scattering (MALS), spettroscopia di assorbimento o fluorescenza, spettrometria di massa o di emissione atomica al plasma accoppiato induttivamente (ICP-MS e ICP-AES, solo per materiali inorganici). Il detector ICP-MS, utilizzato individualmente in modalità single-particle (sp), consente invece di ricavare le dimensioni di nanoparticelle inorganiche come diametro sferico equivalente alla massa. La diffrazione a raggi X (XRD) e la sua derivata small angle X-ray scattering (SAXS) sono altre tecniche ampiamente utilizzate per la caratterizzazione dimensionale di nanomateriali (solamente cristallini nel caso della XRD). La ridotta sensibilità le rende più adatte all’analisi diretta delle materie prime o dei materiali nanocompositi, anziché di campioni alimentari reali, in cui la concentrazione degli analiti è generalmente molto bassa.
Tra le tecniche separative si possono annoverare anche la centrifugal particle sedimentation (CPS) e l’ultracentrifugazione analitica (AUC), che abbinate ad un rivelatore spettrofotometrico forniscono una misura del diametro di sedimentazione di nanoparticelle in sospensione.
Verificare la presenza di un nanomateriale in matrici alimentari, e successivamente determinarne la concentrazione e composizione chimica, è di fondamentale importanza per valutazioni tossicologiche e di ottimizzazione di prodotto/processo. Molte delle tecniche utili a stimare le dimensioni dei nanomateriali consentono anche di ottenere informazioni quantitative, poiché la distribuzione dimensionale si esprime facendo riferimento ad un numero o ad una massa di particelle, o ad un’intensità di segnale. È il caso del DLS e delle tecniche separative, mentre le tecniche di microscopia non sono adatte a valutazioni quantitative. Tra i rivelatori accoppiabili (on-line) o combinabili (off-line) con le tecniche separative, gli strumenti ICP-AES e ancor più ICP-MS offrono la maggiore sensibilità assoluta e precisione nella quantificazione dei nanomateriali inorganici, ricavate misurando la massa degli elementi metallici o semimetallici che li costituiscono. La particle induced X-ray emission (PIXE) e l’ablazione laser (LA)–ICP-MS sono tecniche di imaging particolarmente sensibili per la determinazione di concentrazioni elementari, che in più permettono l’analisi diretta di campioni solidi anche senza particolari preparazioni. Tuttavia, utilizzate da sole sono poco affidabili per campioni reali in quanto non discriminano specie diverse di uno stesso elemento, come ad esempio nanoparticolata e non nanoparticolata. Anche detector basati sulla rifrattometria differenziale (DRI) o sulla spettroscopia UV-vis possono essere accoppiati/combinati con tecniche separative per ottenere dati quantitativi, con sensibilità inferiori alle precedenti, ma offrono il vantaggio di essere applicabili ai nanomateriali sia inorganici che organici.
La composizione chimica di un nanomateriale nella matrice alimentare è un’altra proprietà che consente di verificare la sua corretta identificazione, e di tracciare eventuali trasformazioni nelle matrici alimentari. Tecniche quantitative come ICP-AES/MS e PIXE effettuano misure elemento-specifiche su base spettrale, eventualmente multielementari, e quindi forniscono dati diretti sulla composizione chimica elementare. Tuttavia, con questi rivelatori la certezza di associare univocamente le specie determinate ad un nanomateriale di interesse, senza interferenze della matrice, può essere garantita solo dalla combinazione con una tecnica separativa di provata efficienza per l’applicazione in oggetto.
Diversamente, accoppiando uno spettrometro energy dispersive X-ray (EDS, anche noto come EDX o EDAX) a strumenti di microscopia elettronica a trasmissione (TEM) o scansione (SEM), è possibile ottenere direttamente la composizione elementare (semi-quantitativa) di singoli oggetti nanometrici, anche all’interno di una matrice complessa. L’identificazione di un nanomateriale organico in matrici alimentari è altresì difficile in quanto le sue componenti caratteristiche sono simili a quelle intrinseche della matrice. Per questo motivo, sebbene una grande varietà di tecniche analitiche sia teoricamente utilizzabile per questa determinazione (Tab.2), la loro applicazione spesso non può prescindere da complesse procedure di estrazione e purificazione, risultanti in potenzialmente significative alterazioni degli analiti, e formazione di artefatti analitici.
Sebbene ulteriore ricerca sia necessaria per superare i limiti di molte delle tecniche presentate, le potenzialità analitiche per individuare, caratterizzare e quantificare un nanomateriale in matrici alimentari sono già oggi consistenti. L’approccio ideale deve consentire l’analisi di matrici complesse ed eterogenee, minimizzare la produzione di artefatti derivanti dalla preparazione del campione, e fornire il maggior numero possibile di informazioni mantenendo il minor numero di passaggi operativi. Una strategia di questo tipo può essere realizzata attraverso l’integrazione di più tecniche in grado di produrre dati complementari e reciprocamente confirmatori, organizzate in procedure decisionali che consentano di bilanciare costi e benefici. Lo schema in Figura 1 rappresenta un efficace esempio di tale strategia, finalizzata all’individuazione di un nanomateriale inorganico in matrici alimentari (8).
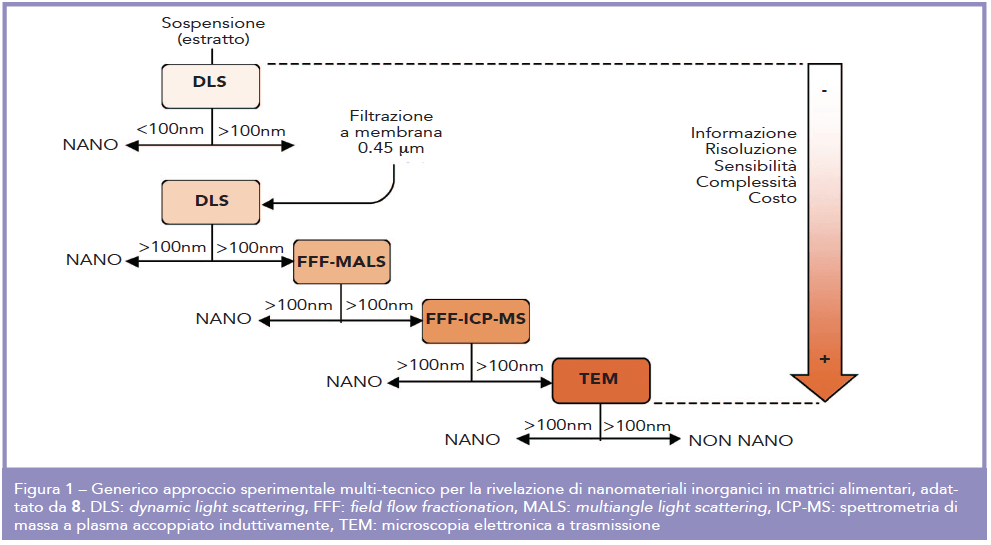
La messa a punto di metodiche analitiche e protocolli operativi standardizzati, applicabili quotidianamente e in grado di rispondere alle nuove normative, è un obiettivo su cui le istituzioni nazionali ed europee e i centri di ricerca stanno investendo molte energie. Le calibrazioni inter-laboratorio per la validazione delle metodiche e lo sviluppo di materiali di riferimento sono una parte fondamentale di queste strategie, cui il Laboratorio ECSIN partecipa attivamente nell’ambito di importanti progetti europei come NanoValid, NANoReg e NANoReg (2).


