Fitosteroli in soggetti ipercolesterolemici over 55
Il consumo di 1,7 g di fitosteroli al giorno da parte degli adulti europei di età superiore ai 55 anni con ipercolesterolemia ridurrebbe del 2,3% il rischio di ospedalizzazione dovuta a eventi cardiovascolari. Ciò comporterebbe risparmi di € 26,5 miliardi nel corso di cinque anni, ovvero € 5,3 miliardi all’anno.
Questi i risultati del nuovo studio commissionato da Food Supplements Europe, (Associazione Europea di Aziende produttrici di Integratori Alimentari), di cui Integratori Italia-AIIPA fa parte, a seguito di un’analisi delle evidenze scientifiche disponibili.
L’ipercolesterolemia è dovuta alla presenza di livelli elevati di colesterolo LDL nel sangue ed è associata ad un più alto rischio di eventi cardiovascolari. In tutta l’UE vivono 31,1 milioni di persone di età superiore a 55 anni che soffrono di ipercolesterolemia grave e che hanno un rischio stimato pari al 24,3% di essere colpiti da un evento cardiovascolare con conseguente ospedalizzazione. I fitosteroli hanno dimostrato di ridurre i livelli di colesterolo LDL. Ci sono prove evidenti che miliardi di euro di costi associati a eventi cardiovascolari potrebbero essere risparmiati attraverso un’integrazione più diffusa tra le popolazioni target nella UE.
I ricercatori indipendenti di Frost & Sullivan hanno calcolato, infatti, l’onere economico legato alla gestione di eventi cardiovascolari dovuti a ipercolesterolemia in questo target di popolazione e hanno stimato un costo a carico dei servizi sanitari dell’UE di 1,328 miliardi di euro tra il 2016 e il 2020, 266 miliardi di euro all’anno, equivalenti a 34637 euro per ogni evento. I risultati dello studio sono riportati nel nuovo rapporto Frost & Sullivan: Healthcare Cost Savings of Phytosterol Food Supplements in the European Union (http://www.foodsupplementseurope.org ).
È il secondo studio pubblicato nell’arco di un anno che ha evidenziato l’enorme potenzialità di una più diffusa integrazione alimentare nella UE nel generare risparmi in relazione a eventi cardiovascolari tra le popolazioni target.
“Nel primo studio, del 2016, i ricercatori di Frost & Sullivan avevano calcolato un risparmio di 13 miliardi di euro all’anno dovuti a malattie cardiovascolari con un consumo giornaliero di 1000 mg di integratori alimentari omega 3 EPA+DHA, nella popolazione over 55”, dichiara Anna Paonessa, Responsabile Integratori Italia – AIIPA. “In questo nuovo studio, si parla sempre di rischio cardiovascolare: l’analisi adesso esamina, attraverso una simulazione, l’impatto positivo dell’integrazione alimentare con fitosteroli sui costi dei servizi sanitari nella UE e sulla qualità di vita del target a rischio, considerato dallo studio.
A febbraio 2017 è stato infine pubblicato un secondo rapporto che aveva calcolato il risparmio generato dall’integrazione di Calcio e Vitamina D nel ridurre le fratture ossee tra i 27,8 milioni di persone dell’UE di età superiore ai 55 anni che soffrono di osteoporosi, per un risparmio valutato di 3,96 miliardi di euro l’anno.
Per informazioni
Angela Sirago, Alessandra Padovan
Ketchum, Ufficio Stampa Integratori Italia
tel 349 2690403
angela.sirago@ketchum.com
tel 02 624119.75
alessandra.padovan@ketchum.com
www.integratoriebenessere.it; www.integratoriitalia.it






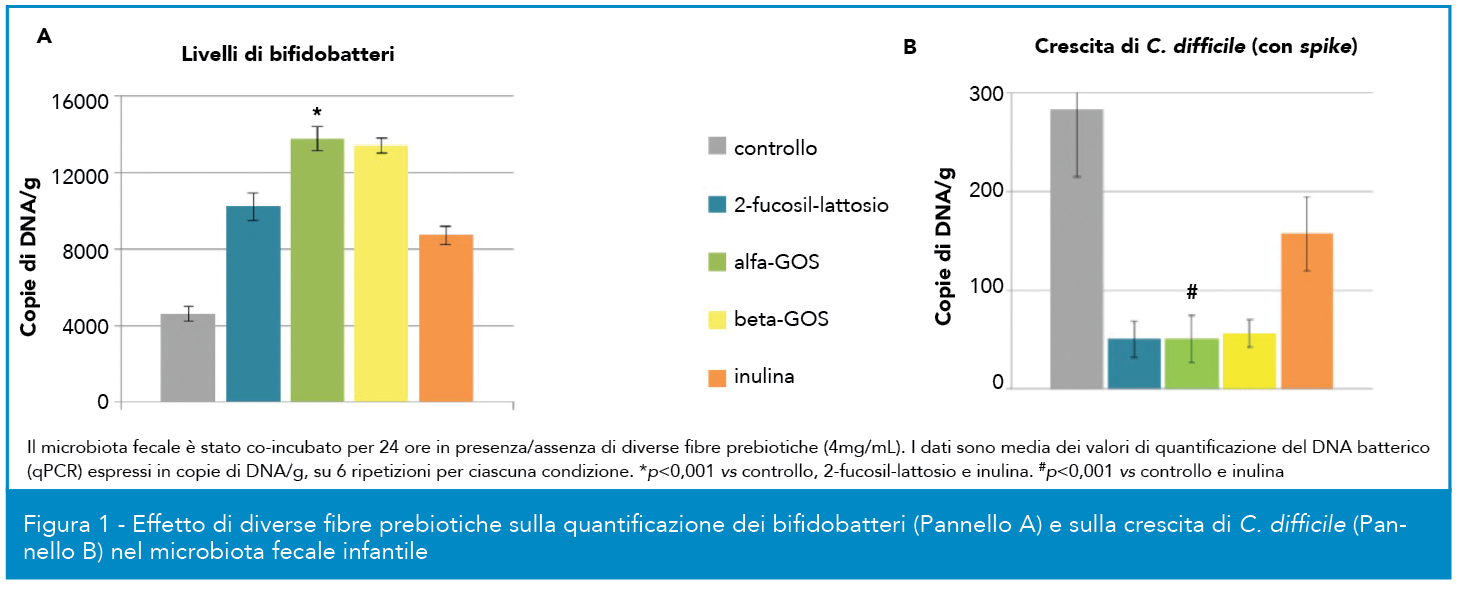
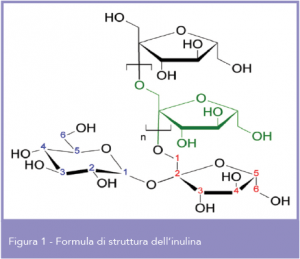 La cicoria (Cichorium intybus) è una pianta erbacea selvatica della famiglia delle Asteraceae, dalle cui radici e parti aeree si ricava un oligosaccaride, l’inulina (Fig.1), polimero glucidico (m.m. ~5000 Da) e fibra vegetale solubile, non assorbita dall’intestino. Tra le varie attività salutistiche attribuite all’inulina, c’è la capacità di prevenire la costipazione e di favorire la motilità intestinale. La costipazione, o stipsi, è una tra le più comuni affezioni nel mondo occidentale. È stato effettuato uno studio clinico (NCT02548247) finalizzato a determinare gli effetti di inulina sulla frequenza della defecazione in soggetti sani affetti da costipazione (3). In questo trial clinico, condotto in base ai recenti documenti di orientamento per la valutazione della funzione intestinale, è stato usato un disegno randomizzato, in doppio cieco, controllato con placebo, cross-over, con 2 settimane di wash out. Ogni periodo dello studio comprendeva una fase di inserimento, seguita dall’assunzione giornaliera di 3 x 4g di inulina x 4 settimane o di maltodestrina. Sono stati arruolati nello studio 44 volontari sani, con costipazione, frequenza e consistenza di evacuazione, caratteristiche gastrointestinali e qualità di vita documentate. Il consumo di inulina ha aumentato significativamente (p=0,038) la frequenza delle evacuazioni (mediana 4,0 [interquartile range (IQR) 2,5-4,5]) vs la malto destrina (3 [IQR 2,5-4,0] evacuazioni/settimana), cui si è aggiunto l’ammorbidimento della consistenza delle feci ed una tendenza verso una maggior soddisfazione rispetto al placebo (p=0,059). Questi risultati dimostrano che l’inulina è efficace in individui con costipazione cronica e migliora significativamente la funzionalità intestinale (3).
La cicoria (Cichorium intybus) è una pianta erbacea selvatica della famiglia delle Asteraceae, dalle cui radici e parti aeree si ricava un oligosaccaride, l’inulina (Fig.1), polimero glucidico (m.m. ~5000 Da) e fibra vegetale solubile, non assorbita dall’intestino. Tra le varie attività salutistiche attribuite all’inulina, c’è la capacità di prevenire la costipazione e di favorire la motilità intestinale. La costipazione, o stipsi, è una tra le più comuni affezioni nel mondo occidentale. È stato effettuato uno studio clinico (NCT02548247) finalizzato a determinare gli effetti di inulina sulla frequenza della defecazione in soggetti sani affetti da costipazione (3). In questo trial clinico, condotto in base ai recenti documenti di orientamento per la valutazione della funzione intestinale, è stato usato un disegno randomizzato, in doppio cieco, controllato con placebo, cross-over, con 2 settimane di wash out. Ogni periodo dello studio comprendeva una fase di inserimento, seguita dall’assunzione giornaliera di 3 x 4g di inulina x 4 settimane o di maltodestrina. Sono stati arruolati nello studio 44 volontari sani, con costipazione, frequenza e consistenza di evacuazione, caratteristiche gastrointestinali e qualità di vita documentate. Il consumo di inulina ha aumentato significativamente (p=0,038) la frequenza delle evacuazioni (mediana 4,0 [interquartile range (IQR) 2,5-4,5]) vs la malto destrina (3 [IQR 2,5-4,0] evacuazioni/settimana), cui si è aggiunto l’ammorbidimento della consistenza delle feci ed una tendenza verso una maggior soddisfazione rispetto al placebo (p=0,059). Questi risultati dimostrano che l’inulina è efficace in individui con costipazione cronica e migliora significativamente la funzionalità intestinale (3).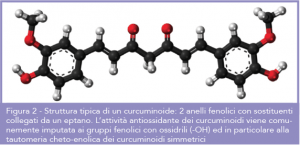 Dal punto di vista farmacodinamico, la curcumina (estratta dalla Curcuma longa) presenta vari target farmacologici e molecolari riconducibili, in genere, all’inibizione di fattori di trascrizione genica coinvolti in processi infiammatori, nonché enzimi, metalli, proteine di trasporto e proteine chinasi. Sono vari e sofisticati gli strumenti di indagine chimico-fisica che hanno permesso di individuare i diversi target molecolari e farmacologici della curcumina e dei suoi metaboliti e/o derivati. Tra questi, la spettroscopia, la risonanza plasmonica di superficie, la competizione legame-ligando, la radiomarcatura, la mutagenesi sito diretta, l’immunoprecipitazione, e molte altre metodiche di ricerca molecolare spesso adoperate per intuire i siti di legame di molecole. Target molecolari della curcumina e dei suoi metaboliti attivi sono diversi e variegati e sfruttano meccanismi di inibizione o di potenziamento, riconducibili a sette macro categorie molecolari: enzimi, proteine chinasi, proteine reduttasi, proteine trasportatrici, molecole pro-infiammatorie, metalli e altro. Lo stress ossidativo ha un ruolo chiave nella patogenesi del diabete mellito (tipo II, DMT2) e nelle complicanze vascolari della patologia. Ciò spiega perché una terapia antiossidante sia suggerita come approccio potenziale per rallentare e smorzare decorso e progressione del DMT2. Scopo di uno studio clinico randomizzato, doppio cieco, controllato con placebo (PLA) è stato valutare gli effetti della supplementazione della dieta di pazienti diabetici di tipo II con curcuminoidi, polifenoli naturali (Fig.2) ottenuti dalla curcuma, sugli indici ossidativi in soggetti diabetici di tipo II. Sono stati arruolati nello studio 118 soggetti affetti da DMT2, randomizzati nei gruppi curcuminoidi (1000 mg/giorno, co-somministrati con piperina (10 mg/giorno), per 8 settimane) e PLA. Capacità antiossidante totale del siero (CATS), attività superossido dismutasi (SOD, enzima antiossidante) e concentrazioni della malonilaldeide (MDA, marker dello stress ossidativo) sono state misurate al tempo 0 e alla fine del periodo di supplementazione. L’assunzione di curcuminoidi ha indotto un aumento significativo delle attività CATS e SOD (p<0,001), mentre i livelli serici di MDA sono risultati significativamente ridotti vs PLA (p<0,001). Questi dati sono rimasti statisticamente significativi anche dopo aggiustamento per potenziali confondenti (differenze della linea di base dell’indice di massa corporea e dell’insulina serica a digiuno). In conclusione, questi risultati supportano l’effetto antiossidante della supplementazione con curcuminoidi in soggetti con DMT2 e incentivano ulteriori studi per valutare l’impatto di questi effetti antiossidanti sull’incidenza delle complicanze diabetiche e degli endpoint cardiovascolari (4).
Dal punto di vista farmacodinamico, la curcumina (estratta dalla Curcuma longa) presenta vari target farmacologici e molecolari riconducibili, in genere, all’inibizione di fattori di trascrizione genica coinvolti in processi infiammatori, nonché enzimi, metalli, proteine di trasporto e proteine chinasi. Sono vari e sofisticati gli strumenti di indagine chimico-fisica che hanno permesso di individuare i diversi target molecolari e farmacologici della curcumina e dei suoi metaboliti e/o derivati. Tra questi, la spettroscopia, la risonanza plasmonica di superficie, la competizione legame-ligando, la radiomarcatura, la mutagenesi sito diretta, l’immunoprecipitazione, e molte altre metodiche di ricerca molecolare spesso adoperate per intuire i siti di legame di molecole. Target molecolari della curcumina e dei suoi metaboliti attivi sono diversi e variegati e sfruttano meccanismi di inibizione o di potenziamento, riconducibili a sette macro categorie molecolari: enzimi, proteine chinasi, proteine reduttasi, proteine trasportatrici, molecole pro-infiammatorie, metalli e altro. Lo stress ossidativo ha un ruolo chiave nella patogenesi del diabete mellito (tipo II, DMT2) e nelle complicanze vascolari della patologia. Ciò spiega perché una terapia antiossidante sia suggerita come approccio potenziale per rallentare e smorzare decorso e progressione del DMT2. Scopo di uno studio clinico randomizzato, doppio cieco, controllato con placebo (PLA) è stato valutare gli effetti della supplementazione della dieta di pazienti diabetici di tipo II con curcuminoidi, polifenoli naturali (Fig.2) ottenuti dalla curcuma, sugli indici ossidativi in soggetti diabetici di tipo II. Sono stati arruolati nello studio 118 soggetti affetti da DMT2, randomizzati nei gruppi curcuminoidi (1000 mg/giorno, co-somministrati con piperina (10 mg/giorno), per 8 settimane) e PLA. Capacità antiossidante totale del siero (CATS), attività superossido dismutasi (SOD, enzima antiossidante) e concentrazioni della malonilaldeide (MDA, marker dello stress ossidativo) sono state misurate al tempo 0 e alla fine del periodo di supplementazione. L’assunzione di curcuminoidi ha indotto un aumento significativo delle attività CATS e SOD (p<0,001), mentre i livelli serici di MDA sono risultati significativamente ridotti vs PLA (p<0,001). Questi dati sono rimasti statisticamente significativi anche dopo aggiustamento per potenziali confondenti (differenze della linea di base dell’indice di massa corporea e dell’insulina serica a digiuno). In conclusione, questi risultati supportano l’effetto antiossidante della supplementazione con curcuminoidi in soggetti con DMT2 e incentivano ulteriori studi per valutare l’impatto di questi effetti antiossidanti sull’incidenza delle complicanze diabetiche e degli endpoint cardiovascolari (4). La steatosi epatica, patologia cellulare legata all’accumulo di trigliceridi (steatosi) negli epatociti, è un processo degenerativo che può comportare una serie di gravi danni fino alla necrosi del parenchima epatico e all’insufficienza epatica. Ci sono evidenze scientifiche che la somministrazione di olio di Rosa mosqueta (RM) (Fig.3) prevenga la steatosi epatica. L’olio di questa rosa selvatica è ricco di acido α-linolenico (ALA), precursore degli acidi eicosapentaenoico (EPA) e docosaesaenoico (DHA), mentre l’elevato contenuto in tocoferoli gli conferisce una forte attività antiossidante. Allo scopo di dimostrare il meccanismo antilipogenico indotto dalla somministrazione di olio di RM, in un modello murino alimentato con dieta ad alto contenuto di grassi, è stato fatto uno studio di valutazione dei marker associati alla regolazione del metabolismo delle lipid droplet protein (Plin2 (adipose differentiation-related protein), Plin5 (myocardial lipid droplet protein) e PPAR-γ (peroxisome proliferator-activated receptor gamma)) e delle proteine associate alla lipogenesi: fatty acid synthetase (FAS) e sterol regulatory element binding protein-1c (SREBP-1c). I topi sono stati alimentati, per 12 settimane, con dieta di controllo (CON) o con dieta a elevato contenuto di grassi (HFD), con e senza supplementazione di olio di RM (4 gruppi sperimentali). I risultati dimostrano che l’integrazione di olio di RM diminuisce l’espressione epatica dell’mRNA di PLIN2 e PPAR-γ e i livelli delle proteine SREBP-1c, FAS e PLIN2, mentre non indicano cambiamenti dei livelli di PLIN5 nei 4 gruppi di topi. Questi risultati permettono di ipotizzare che la modulazione dei marker lipogenici potrebbe essere uno dei meccanismi attraverso i quali l’integrazione con olio di RM previene, in un modello murino, la steatosi epatica indotta dal consumo di una dieta ricca di grassi (8).
La steatosi epatica, patologia cellulare legata all’accumulo di trigliceridi (steatosi) negli epatociti, è un processo degenerativo che può comportare una serie di gravi danni fino alla necrosi del parenchima epatico e all’insufficienza epatica. Ci sono evidenze scientifiche che la somministrazione di olio di Rosa mosqueta (RM) (Fig.3) prevenga la steatosi epatica. L’olio di questa rosa selvatica è ricco di acido α-linolenico (ALA), precursore degli acidi eicosapentaenoico (EPA) e docosaesaenoico (DHA), mentre l’elevato contenuto in tocoferoli gli conferisce una forte attività antiossidante. Allo scopo di dimostrare il meccanismo antilipogenico indotto dalla somministrazione di olio di RM, in un modello murino alimentato con dieta ad alto contenuto di grassi, è stato fatto uno studio di valutazione dei marker associati alla regolazione del metabolismo delle lipid droplet protein (Plin2 (adipose differentiation-related protein), Plin5 (myocardial lipid droplet protein) e PPAR-γ (peroxisome proliferator-activated receptor gamma)) e delle proteine associate alla lipogenesi: fatty acid synthetase (FAS) e sterol regulatory element binding protein-1c (SREBP-1c). I topi sono stati alimentati, per 12 settimane, con dieta di controllo (CON) o con dieta a elevato contenuto di grassi (HFD), con e senza supplementazione di olio di RM (4 gruppi sperimentali). I risultati dimostrano che l’integrazione di olio di RM diminuisce l’espressione epatica dell’mRNA di PLIN2 e PPAR-γ e i livelli delle proteine SREBP-1c, FAS e PLIN2, mentre non indicano cambiamenti dei livelli di PLIN5 nei 4 gruppi di topi. Questi risultati permettono di ipotizzare che la modulazione dei marker lipogenici potrebbe essere uno dei meccanismi attraverso i quali l’integrazione con olio di RM previene, in un modello murino, la steatosi epatica indotta dal consumo di una dieta ricca di grassi (8).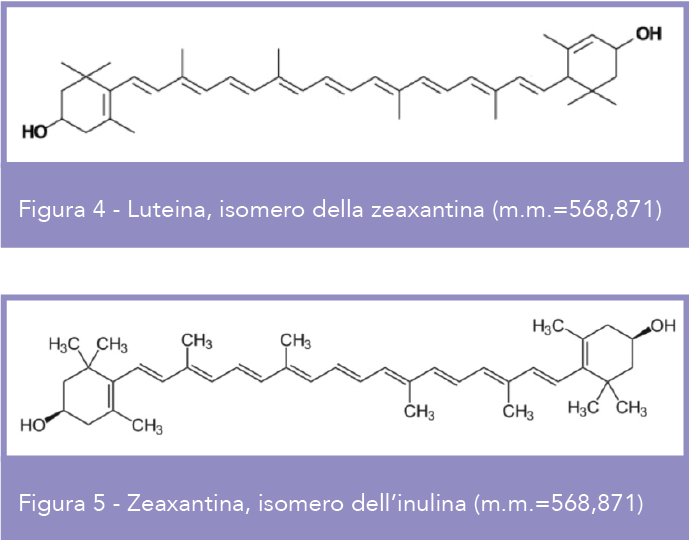 Luteina (LU) e zeaxantina (ZE) sono carotenoidi alimentari con effetti salutistici in alcuni disturbi visivi e cognitivi. La LU (Fig.4) è una xantofilla corrispondente al β-carotene, con due gruppi ossidrilici negli anelli terminali. I petali dei fiori di Tagetes erecta sono la fonte principale di LU. La ZE, xantofilla (Fig.5) isomero della luteina, si trova nel mais, nel tuorlo d’uovo, nel peperone rosso, nel mango e nell’arancia. Ambedue le xantine, presenti anche in vegetali a foglia verde scura, formano il pigmento naturale dell’occhio umano. Una review recente (11) fa il punto sulle conoscenze relative agli effetti farmacologici indotti dalla supplementazione della dieta con questi due integratori naturali. Si è ipotizzato che LU e ZE esercitino un’azione protettiva in patologie della vista, quali la degenerazione maculare senile (DMS), la cataratta senile (CS), la retinopatia indotta da ipossia ischemica, leggeri danni della retina, la retinite pigmentosa, il distacco retinico, l’uveite e la retinopatia diabetica, e nelle patologie cognitive. Il/i meccanismo/i, grazie al/i quale/i questi carotenoidi sono coinvolti nella prevenzione delle patologie oculari, può essere in qualche modo legato alle loro proprietà di filtrazione della luce blu e ad attività antiossidante locale. Oltre al loro ruolo protettivo dal danno ossidativo indotto dalla luce, evidenze sempre più numerose indicano che LU e ZE possano anche migliorare la normale funzione visiva, aumentando la sensibilità al contrasto di luce e riducendo la disabilità da abbagliamento. Valutazioni sulla supplementazione con LU e ZE indicano che assunzioni moderate di queste sostanze sono associate a un ridotto rischio di DMS e a un minore danno visivo. Questa review prende in esame le quantità più appropriate di consumo, la sicurezza dell’assunzione di LU, i relativi effetti collaterali oltre alle future linee di ricerca (11).
Luteina (LU) e zeaxantina (ZE) sono carotenoidi alimentari con effetti salutistici in alcuni disturbi visivi e cognitivi. La LU (Fig.4) è una xantofilla corrispondente al β-carotene, con due gruppi ossidrilici negli anelli terminali. I petali dei fiori di Tagetes erecta sono la fonte principale di LU. La ZE, xantofilla (Fig.5) isomero della luteina, si trova nel mais, nel tuorlo d’uovo, nel peperone rosso, nel mango e nell’arancia. Ambedue le xantine, presenti anche in vegetali a foglia verde scura, formano il pigmento naturale dell’occhio umano. Una review recente (11) fa il punto sulle conoscenze relative agli effetti farmacologici indotti dalla supplementazione della dieta con questi due integratori naturali. Si è ipotizzato che LU e ZE esercitino un’azione protettiva in patologie della vista, quali la degenerazione maculare senile (DMS), la cataratta senile (CS), la retinopatia indotta da ipossia ischemica, leggeri danni della retina, la retinite pigmentosa, il distacco retinico, l’uveite e la retinopatia diabetica, e nelle patologie cognitive. Il/i meccanismo/i, grazie al/i quale/i questi carotenoidi sono coinvolti nella prevenzione delle patologie oculari, può essere in qualche modo legato alle loro proprietà di filtrazione della luce blu e ad attività antiossidante locale. Oltre al loro ruolo protettivo dal danno ossidativo indotto dalla luce, evidenze sempre più numerose indicano che LU e ZE possano anche migliorare la normale funzione visiva, aumentando la sensibilità al contrasto di luce e riducendo la disabilità da abbagliamento. Valutazioni sulla supplementazione con LU e ZE indicano che assunzioni moderate di queste sostanze sono associate a un ridotto rischio di DMS e a un minore danno visivo. Questa review prende in esame le quantità più appropriate di consumo, la sicurezza dell’assunzione di LU, i relativi effetti collaterali oltre alle future linee di ricerca (11).


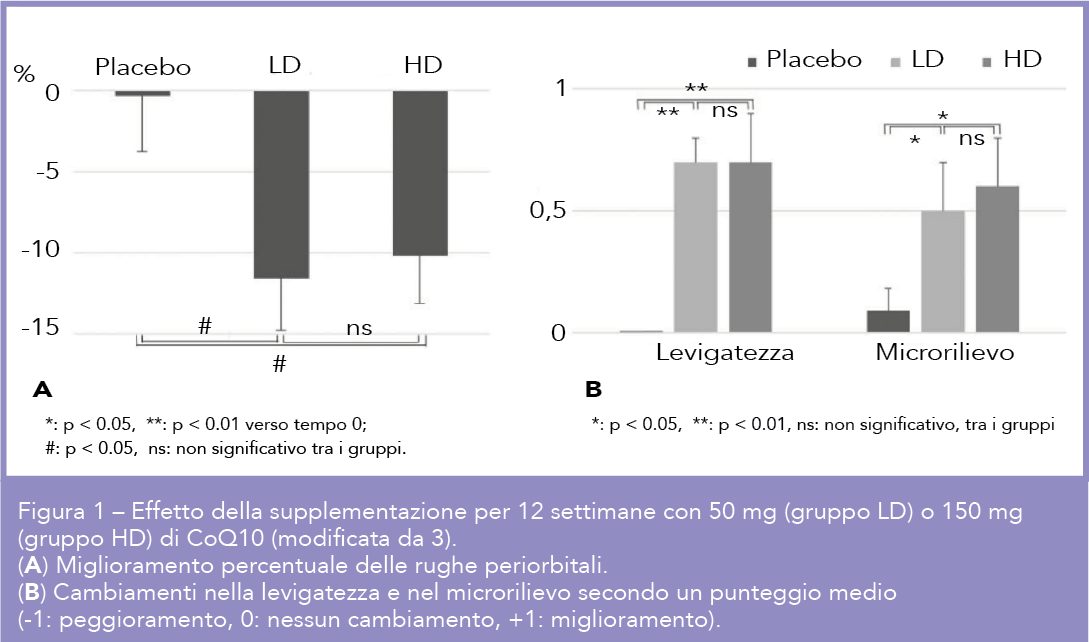 e rughe periorbitali e il microrilievo sono migliorati (Fig. 1) allo stesso modo sia nel gruppo LD che HD, mentre le pieghe nasolabiali, le rughe degli angoli della bocca e periorali sono migliorate solo nel gruppo HD. Sarebbe stato interessante che fossero state pubblicate non solo le foto della regione periorbitale ma anche quelle della regione periorale per poter valutare i miglioramenti in una zona di fondamentale importanza, sia per l’estetica che per il make up. Un’altra limitazione dello studio che si è svolto tra novembre e gennaio, oltre al basso numero di partecipanti che come sottolineato anche dagli Autori avrebbe dovuto avere almeno 100 soggetti per gruppo, è stata la breve durata del trattamento: non si sono potuti valutare così i cambiamenti dei parametri cutanei al variare delle stagioni e non si è permesso che si esplicassero appieno gli effetti della supplementazione orale (che richiede più cicli cutanei); forse si sarebbero potuti così osservare gli effetti sulla produzione e sulla diminuita degradazione delle proteine strutturali del derma, come il collagene e l’elastina, che si sono viste in alcuni studi in vitro. Lo svolgimento dello studio nella stagione fredda ha comunque evidenziato l’effetto del CoQ10 nel limitare gli effetti negativi dei mesi invernali su parametri cutanei come l’elasticità. Non essendo stato rilevato alcun cambiamento nell’idratazione cutanea si può dedurre che l’effetto del CoQ10 si sia esplicato soprattutto a livello dermico e che la quantità escreta sulla superfice cutanea, tramite il sebo ai dosaggi utilizzati, non influisca su questo parametro. Inoltre va sottolineato che i miglioramenti sono stati notati non solo dai dermatologi esperti ma anche dalle partecipanti, nelle percentuali del 70, 36 e 18% rispettivamente nel gruppo HD, LD e placebo. È noto come l’effetto antiaging possa essere ottenuto sostenendo il metabolismo energetico cellulare non solo con il CoQ10 ma anche con la creatina. La via della creatina-fosfocreatina rende rapidamente disponibile l’ATP in caso di bisogno improvviso, come nell’ipossia e nell’anossia, e in quei casi in cui si debbano riparare i danni cellulari provocati dallo stress ossidativo. Nella cute anche i livelli di creatina come quelli di CoQ10 diminuiscono con l’età. Uno studio (4) ha mostrato infatti come l’applicazione topica di acido folico e creatina abbia migliorato i segni dell’aging cutaneo in vivo aumentando i livelli di procollagene e migliorando la densità del collagene. Nella formulazione di prodotti ad azione antiaging potrebbe essere utilizzata l’azione sinergica del CoQ10 e della creatina per mantenere i livelli energetici cutanei e contrastare i segni del cronoaging.
e rughe periorbitali e il microrilievo sono migliorati (Fig. 1) allo stesso modo sia nel gruppo LD che HD, mentre le pieghe nasolabiali, le rughe degli angoli della bocca e periorali sono migliorate solo nel gruppo HD. Sarebbe stato interessante che fossero state pubblicate non solo le foto della regione periorbitale ma anche quelle della regione periorale per poter valutare i miglioramenti in una zona di fondamentale importanza, sia per l’estetica che per il make up. Un’altra limitazione dello studio che si è svolto tra novembre e gennaio, oltre al basso numero di partecipanti che come sottolineato anche dagli Autori avrebbe dovuto avere almeno 100 soggetti per gruppo, è stata la breve durata del trattamento: non si sono potuti valutare così i cambiamenti dei parametri cutanei al variare delle stagioni e non si è permesso che si esplicassero appieno gli effetti della supplementazione orale (che richiede più cicli cutanei); forse si sarebbero potuti così osservare gli effetti sulla produzione e sulla diminuita degradazione delle proteine strutturali del derma, come il collagene e l’elastina, che si sono viste in alcuni studi in vitro. Lo svolgimento dello studio nella stagione fredda ha comunque evidenziato l’effetto del CoQ10 nel limitare gli effetti negativi dei mesi invernali su parametri cutanei come l’elasticità. Non essendo stato rilevato alcun cambiamento nell’idratazione cutanea si può dedurre che l’effetto del CoQ10 si sia esplicato soprattutto a livello dermico e che la quantità escreta sulla superfice cutanea, tramite il sebo ai dosaggi utilizzati, non influisca su questo parametro. Inoltre va sottolineato che i miglioramenti sono stati notati non solo dai dermatologi esperti ma anche dalle partecipanti, nelle percentuali del 70, 36 e 18% rispettivamente nel gruppo HD, LD e placebo. È noto come l’effetto antiaging possa essere ottenuto sostenendo il metabolismo energetico cellulare non solo con il CoQ10 ma anche con la creatina. La via della creatina-fosfocreatina rende rapidamente disponibile l’ATP in caso di bisogno improvviso, come nell’ipossia e nell’anossia, e in quei casi in cui si debbano riparare i danni cellulari provocati dallo stress ossidativo. Nella cute anche i livelli di creatina come quelli di CoQ10 diminuiscono con l’età. Uno studio (4) ha mostrato infatti come l’applicazione topica di acido folico e creatina abbia migliorato i segni dell’aging cutaneo in vivo aumentando i livelli di procollagene e migliorando la densità del collagene. Nella formulazione di prodotti ad azione antiaging potrebbe essere utilizzata l’azione sinergica del CoQ10 e della creatina per mantenere i livelli energetici cutanei e contrastare i segni del cronoaging.